一种基于四面体框架核酸的复合佐剂、mRNA疫苗及其制备方法和用途
2024-06-26
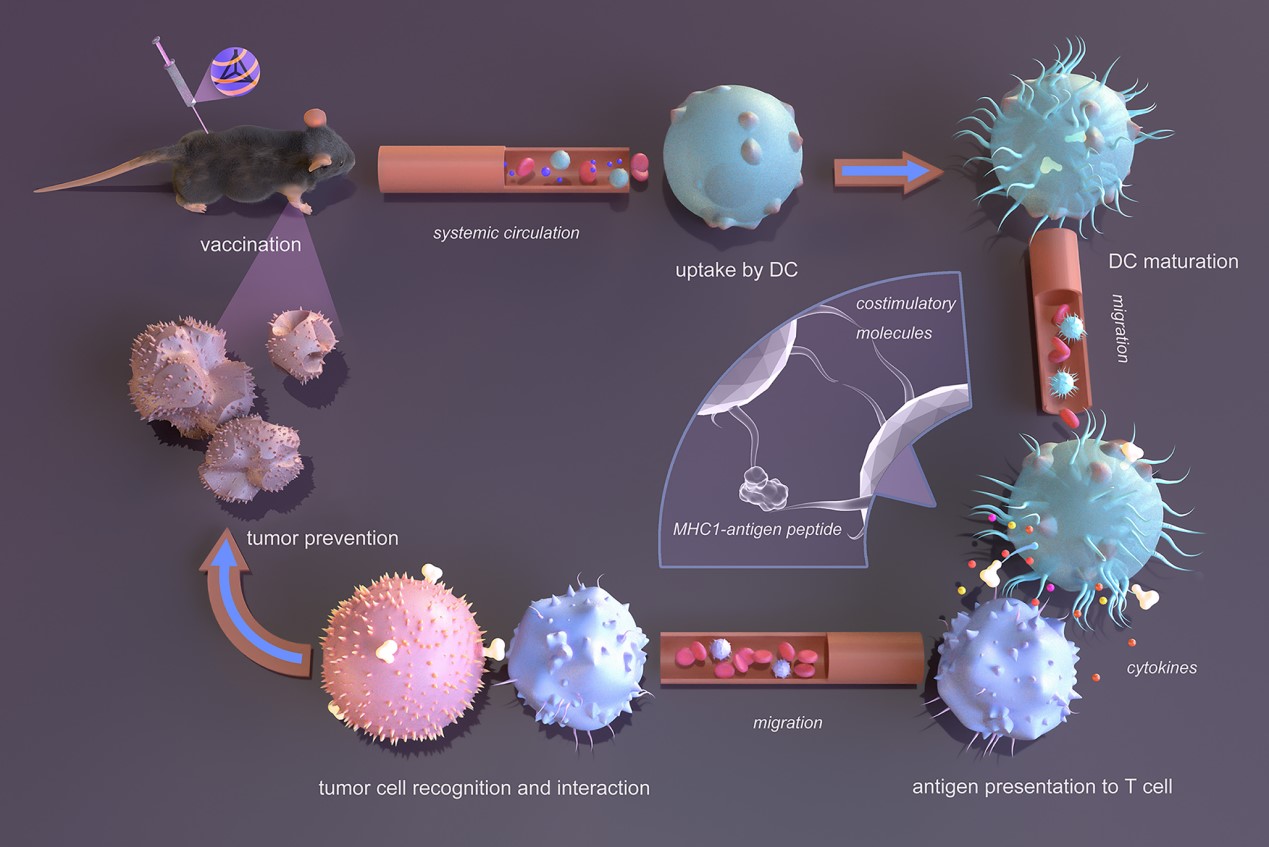
本发明提供了一种CpG‑tFNA和mDF2β的复合佐剂,以及基于该复合佐剂的mRNA纳米疫苗;mRNA在没有佐剂的情况下几乎不会进入细胞发挥功能,而使用本发明复合佐剂的mRNA纳米疫苗不但生物安全性好,而且可被树突状细胞内化并促进其成熟,成熟的树突状细胞分泌细胞因子并在细胞膜上表达共刺激分子,随后迁移并与T细胞接触以进行抗原呈递;活化的抗原特异性CD8+T细胞迁移至外周,浸润早期肿瘤组织,识别和攻击肿瘤细胞,最终抑制肿瘤的发生和生长,两种佐剂复合起到了协同增效作用,比仅使用一种佐剂的mRNA纳米疫苗具有更好的效果,应用前景优异。
背景:
核酸疫苗在多类疾病的预防和治疗中显示出巨大的前景。其关键优势在于优先刺激细胞免疫而不是体液免疫。这是因为内源性抗原由MHC1类分子介导抗原呈递,导致CD8阳性T细胞的活化,从而促进细胞免疫。此外,核酸序列易于体外扩增,使得快速量产核酸疫苗的可行性较高。核酸疫苗中的mRNA疫苗通常在蛋白质翻译后受到降解,具有很高的生物安全性。目前已有较多研究意识到了mRNA疫苗的优点,并在初期临床阶段成功验证了mRNA疫苗的功效。例如新型冠状病毒的mRNA疫苗;此外,诸多mRNA疫苗正在针对多种肿瘤进行临床试验,如黑色素瘤和前列腺癌。但是,mRNA疫苗的广泛应用仍然面临挑战。mRNA是核苷酸的长链状聚合物,带负电荷,若没有载体递送,易导致细胞通透性差。此外,单链mRNA的稳定性较差,人工合成时通常需要特定核酸(例如5‑甲基胞苷)的修饰以提高稳定性。然而,这一类的修饰往往降低了mRNA自身的佐剂效应,从而削弱了对抗原呈递细胞的活化的刺激能力。目前,脂质体载体被广泛使用于mRNA的递送,但具有一系列潜在缺点,例如体内毒性,对抗原呈递细胞缺乏靶向性,以及难以共同递送多种佐剂。对于mRNA药物而言,理想的载体及佐剂应至少满足以下特征:(1)增强mRNA的递送;(2)有效激活免疫细胞,尤其是抗原呈递细胞;(3)优先诱导细胞免疫而非体液免疫;(4)非特异性免疫低;(5)不引起体内毒性;但目前兼具上述优异特性的mRNA疫苗佐剂还鲜有报道。
前沿科研成果:基于四面体框架核酸的复合佐剂、mRNA疫苗用于肿瘤预防
在新兴的纳米材料中,我们关注到四面体框架核酸(tetrahedral framework nucleic acid, tFNA)是一种极富前景的三维核酸纳米材料,具有优异的细胞通透性和生物安全性。先前的研究表明,tFNA可通过非常简捷的序列延伸等方式,成功负载多类寡核苷酸药物,并显著提高其体内外递送效率。譬如,tFNA可以在其四个顶点上全部负载经典免疫佐剂CpG序列,进而显著促进CpG序列的细胞摄取和免疫刺激能力。
另一方面, 宿主防御肽(host defense peptide, HDP)是一种内源性功能分子,最早因抗菌活性而受到关注,近年来逐渐被定位为多功能的免疫调节分子,例如招募和激活免疫细胞。作为一种有代表性的HDP,mDF2β作用于DC的细胞膜受体,Toll样受体4(Toll-like receptor 4, TLR4),以激活特异性免疫。目前常见的纳米疫苗通常依赖其特定的几何和电荷性质,例如球形和带正电荷,以实现对抗原呈递细胞的被动靶向性摄取,而mDF2β的独特优势是对DC细胞具有主动靶向性,因为其受体TLR4位于DC细胞的细胞膜上。此外,mDF2β为正电性分子,可以基于静电相互作用而便捷地与负电性的mRNA或其它纳米材料(例如tFNA)复合。尽管存在这些优势,目前尚未见国内外学者将mDF2β或者其它的HDP分子用作mRNA纳米疫苗的佐剂成分。
在此,旨在开发一种由CpG-tFNA和mDF2β共同组成的新型双佐剂制剂,应用于复合mRNA纳米疫苗的制备,并评估其肿瘤预防性能。
研究方法:
采用AFM、TEM、PAGE等方法鉴定纳米疫苗的合成;共聚焦显微镜和流式细胞术检测树突状细胞对疫苗的摄取效率;流式细胞术、ELISA、扫描电镜等测定树突状细胞的激活与成熟;活体成像、流式细胞术等验证疫苗对活体的免疫激活效果;动物实验(T细胞淋巴瘤)评估疫苗的肿瘤预防作用。
实验结果:
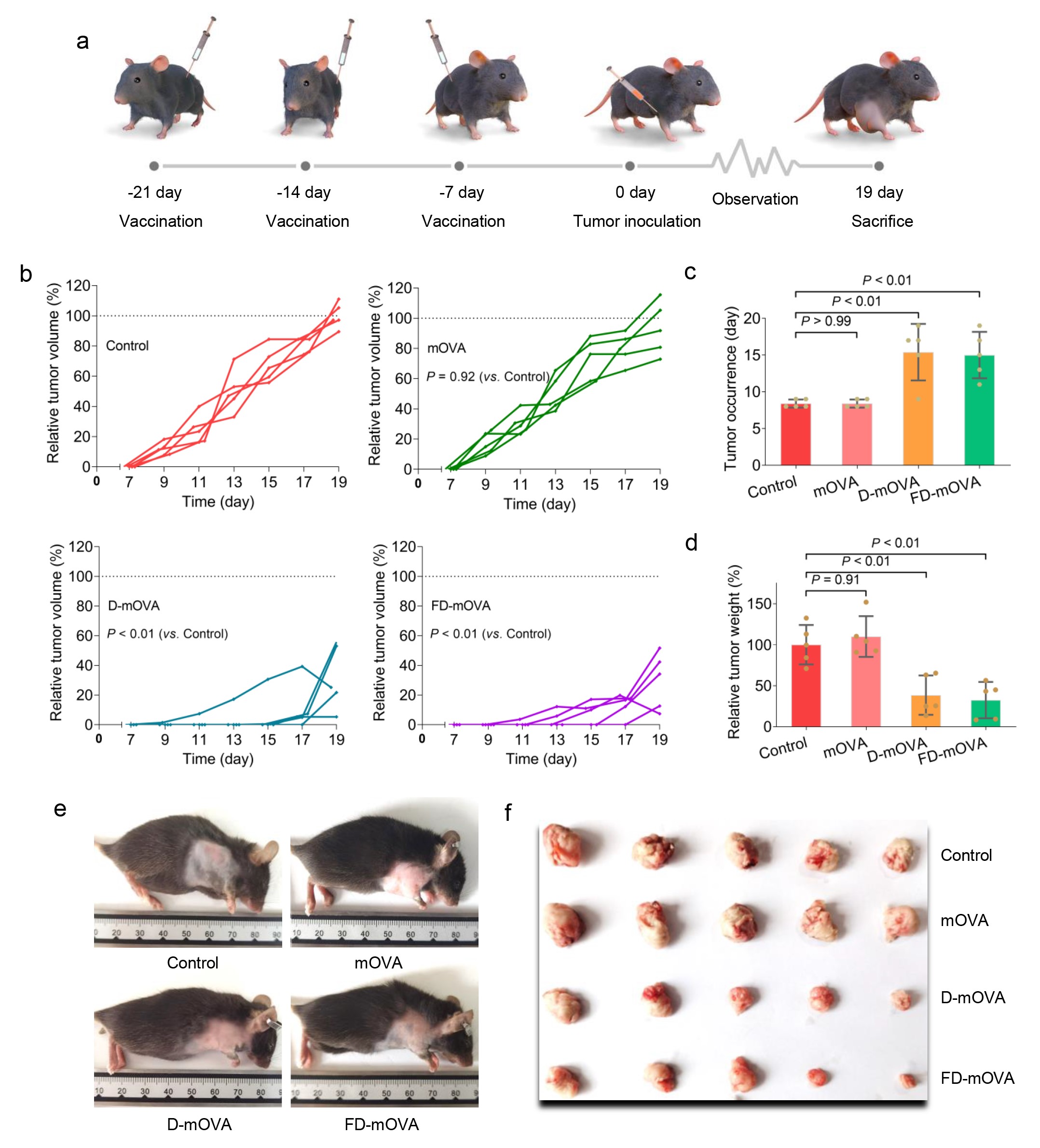
技术团队成功研发了双佐剂mRNA纳米疫苗。该疫苗能够增加树突状细胞对mRNA的摄取,促进树突状细胞的成熟以及抗原的表达和呈递,并进一步诱导T细胞介导的细胞免疫。在肿瘤预防性接种模型中,双佐剂mRNA纳米疫苗表现出优异的抗肿瘤效果,宏观表现为肿瘤发生的延迟和肿瘤体积的减少,微观表现为T细胞浸润面积的增加和肿瘤组织凋亡及坏死面积的增加。此外,本研究未发现该纳米疫苗产生明显毒副作用。
研究结论:
技术团队研发了一种基于四面体框架核酸、宿主防御肽的双佐剂mRNA纳米疫苗,兼具优异的免疫效力及生物安全性,对于mRNA纳米疫苗技术有着深远的应用前景,尤其是肿瘤和病毒性疾病的预防和治疗。
发表文献:Chinese Chem Lett. 2023, 34(7), 107987, IF=9.1 DOI: 10.1016/j.cclet.2022.107987