一种基于框架核酸材料的microRNA纳米复合体及其制备方法和用途
2024-06-26
微小RNA(miRs)在调节基因表达方面发挥着重要作用。受其不稳定性的限制,miR疗法需要递送载体。四面体骨架核酸(tFNA)可能适用于药物递送,因为它们显著穿透组织并被细胞吸收。然而,基于tFNA的miR递送策略未能在miR进入细胞后将其分离,影响了miR的效率。在这项研究中,应用RNase H响应序列连接粘性末端tFNA(stFNA)和miR-2861(一种模型miR),以靶向骨髓间充质干细胞中组蛋白去乙酰化酶5(HDAC5)的表达。由此产生的生物可切换纳米复合物(stFNA-miR)能够在细胞内递送后有效地卸载和部署miR-2861,从而抑制HDAC5的表达并促进成骨分化。stFNA-miR还通过局部注射促进理想的骨修复。总之,一种通用的miR递送策略可用于需要调节基因表达的各种生物医学应用。
背景:
基于Watson-Crick杂交原则,DNA具有良好的可编辑性,这也使得DNA纳米技术在1982年首次被提出以来,能够在各种领域飞速发展并应用广泛。由于DNA纳米结构具有良好的生物学稳定性与生物相容性,可编辑性以及出色的穿透细胞膜能力,使得DNA纳米结构能够在药物运输领域具有巨大的应用潜力。在DNA纳米结构中,四面体DNA纳米结构显示出了极为优秀的运载药物能力。目前已被证实的是,四面体DNA框架核酸结构(tFNA),既能够运输具有中性电荷的肽核酸,也能运输带有负电荷的DNA和RNA。作为目前已成功合成的最简单的DNA纳米结构,tFNA能够以小窝蛋白依赖的方式被细胞内吞,最终将所装载的“货物”运输到细胞内部。
核酸药物是具有不同功能的RNA或DNA作用于目标mRNA,从转录后水平进行基因沉默来起到治疗效果,核酸药物具有高特异性,高效性,长效性等明显优势。MicroRNA(miRNAs)能与mRNA相作用而调控着细胞内生化反应的发生。每个miRNA可以调控多个靶基因,而几个miRNA也可以共同调节同一个基因。这样就形成了一个错综复杂的调解网络,因此miRNA目前也被证实参与着几乎所有人体内的生命调节。因此miRNA在核酸药物领域的具有巨大的应用潜力。即便拥有功能多样性,然而由于miRNA的单链结构,其自身的不稳定性也大大限制了它的应用范围。作为一种高效安全的药物递送系统,tFNAs具有良好的生物相容性及穿过细胞膜的特性,因此将miRNA装载在tFNAs上运输进入细胞或许能打破不稳定性对于miRNA应用上的限制。在先前的研究中,我们技术团队曾通过合成miRNA-DNA混合核酸序列来组装出装载有miRNA的tFNAs。并且通过这种方式也成功的观察到了这种纳米复合体进入细胞后发挥作用。然而由于所装载的miRNA为单链结构,与双链结构的miRNA相比,单链的miRNA结构稳定性较差。除此之外,这种运输方式是将miRNA通过磷酸二酯键连接在tFNAs上的,在进入细胞后,所运输的miRNA在细胞内将会组成RNA-induced silencing complex(RISC)来发挥作用,而运载体的存在可能影响miRNA在细胞内的作用效率。
前沿科研成果:一种基于框架核酸材料的microRNA纳米复合体及其制备方法和用途
微小RNA(miRs)在调控基因表达方面发挥着重要作用。但由于其不稳定性,miR治疗需要载体。四面体框架核酸(tFNAs)因其能显著穿透组织并被细胞吸收而可能适用于药物递送。然而,基于tFNA的miR递送策略在miR进入细胞后未能将其分离,影响了miR的效率。在这项研究中,将RNase H响应序列应用于连接黏性末端tFNA(stFNA)和模型miR-2861,以靶向骨髓间充质干细胞中组蛋白脱乙酰酶5(HDAC5)的表达。由此产生的生物可开关纳米复合物(stFNA-miR)可在细胞内递送后高效卸载和部署miR-2861,从而抑制HDAC5的表达并促进成骨分化。stFNA-miR还通过局部注射促进了理想的骨修复。总之,提供了一种适用于各种需要调节基因表达的生物医学应用的通用miR递送策略。
研究方法:
采用AFM、TEM、和PAGE等方法鉴定stFNA-miR的合成;共聚焦显微镜和流式细胞术检测stFNA-miR进入软骨细胞的能力;CCK8和流式细胞术检测stFNA-miR进入BMSCs的情况;qPCR、WB检测stFNA-miR对成骨相关基因和蛋白的调控。动物实验检测stFNA-miR在体内水平的骨修复作用。
实验结果:
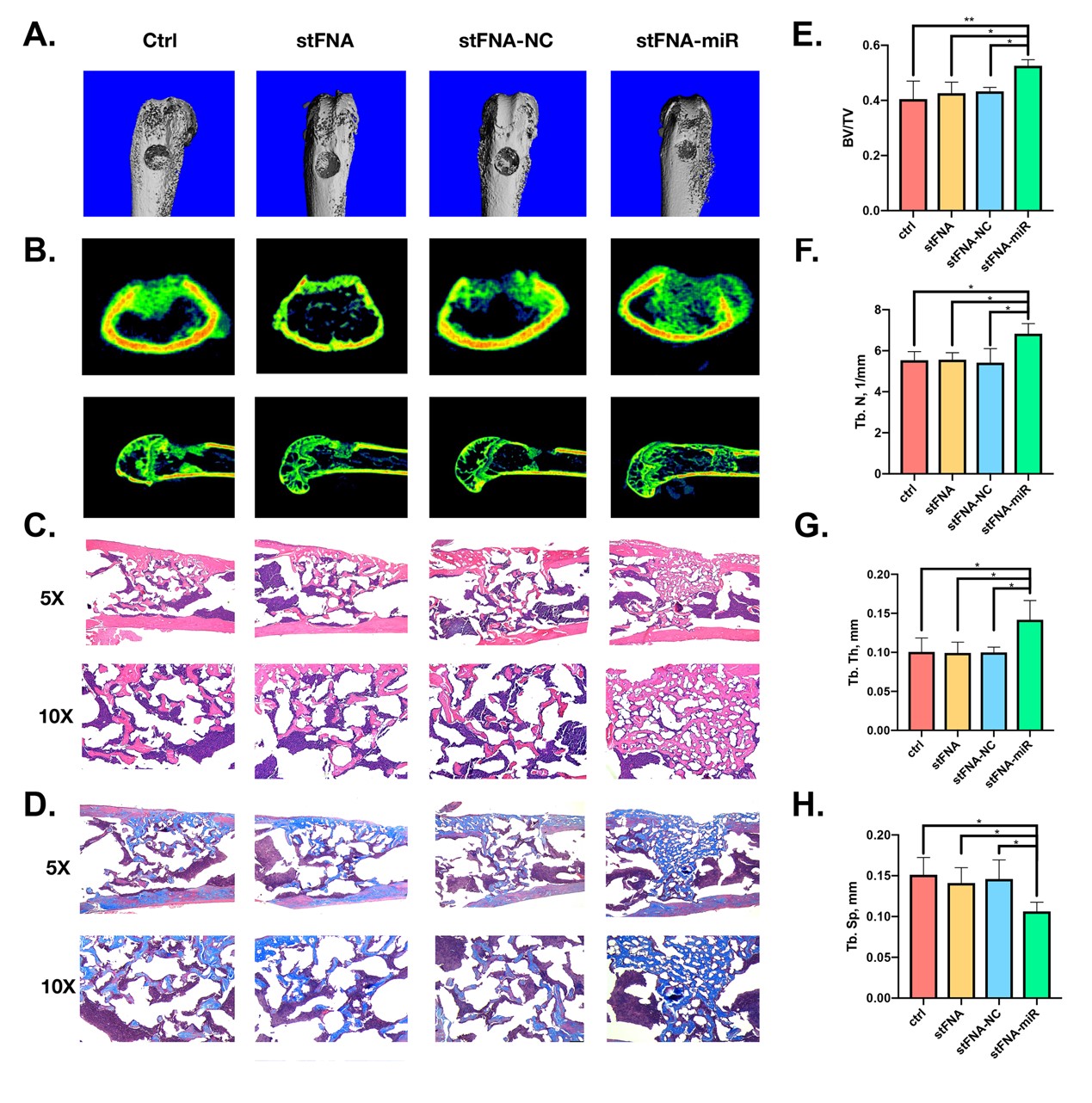
我们技术团队成功合成了stFNA-miR并对其进行了表征。本纳米复合体证实在翻译水平抑制histone deacetylase 5 (HDAC5)蛋白的表达,从而使runtrelated transcription factor 2 (Runx2)蛋白表达上调,最终促进BMSC细胞发生成骨向分化。除此之外,我们技术团队也将stFNA-miR应用到小鼠体内模型中,来观察其在体内的骨再生效果及药物毒性反应。这一运输模式能够将功能性极为多样的miRNA应用于众多领域,除了本研究所涉及的组织再生领域之外,还可以将这一运输模式应用在肿瘤靶向治疗、抗菌治疗、基因诊断等多生物医药领域。
研究结论:
我们的技术团队成功地构建了一种用于生物可开关的 miRNA 递送系统,其能在没有转染试剂的情况下,能够大量进入到BMSCs中,并成功实现miRNA的卸载,在相应的骨修复体内以及体外实验中均观察到了出色的效果。
发表文献:Small. 2021, 2104359 ,IF=13 DOI: 10.1002/smll.2104359
![]() Bioswitchable Delivery of microRNA by Framework Nucleic Acids: Application to Bone Regeneration
Bioswitchable Delivery of microRNA by Framework Nucleic Acids: Application to Bone Regeneration