DNA四面体在制备预防和治疗1型糖尿病的药物中的用途
2024-06-26
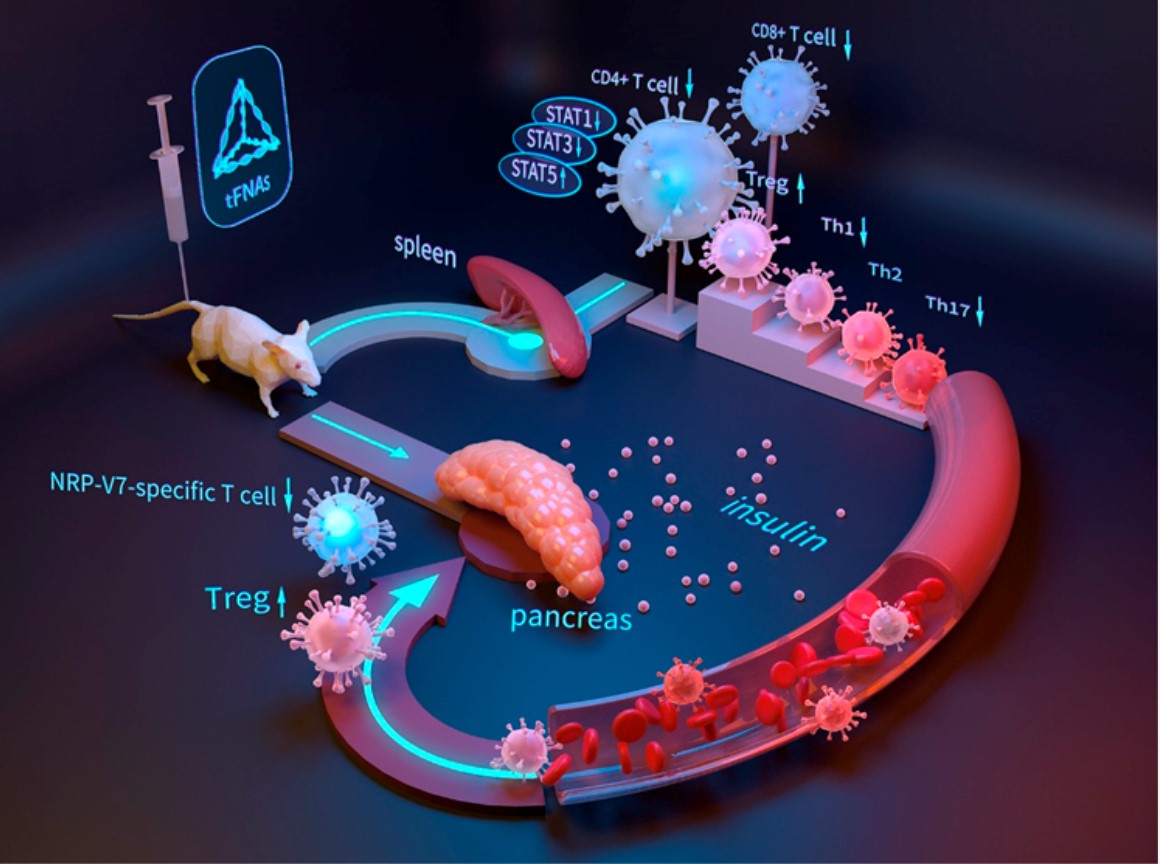
免疫耐受的失败导致胰岛素产生的β细胞自身免疫破坏,进而导致1型糖尿病(T1D)。抑制自身反应性T细胞并诱导调节性T细胞(Tregs)以重新建立免疫耐受是预防T1D发病的有前景的方法。在这里,我们研究了四面体框架核酸(tFNAs)诱导免疫耐受并预防非肥胖型糖尿病(NOD)小鼠T1D的能力。在糖尿病前期的NOD小鼠中,tFNAs治疗导致血糖维持正常,并减少了糖尿病的发生率。此外,tFNAs(250 nM)治疗保护了β细胞的质量和功能,增加了Tregs的频率,并抑制了自身反应性T细胞,从而导致免疫耐受。总体而言,我们的结果表明,tFNAs治疗有助于血糖控制,提供β细胞保护,并通过免疫调节预防了NOD小鼠T1D的发病。这些结果突显了tFNAs在预防自身免疫性T1D中的潜力。
背景:
在本研究中,我们探讨了四面体框架核酸(tFNAs)在预防1型糖尿病(T1D)中的应用。T1D是一种严重的自身免疫性疾病,全球数百万人受其影响,表现为免疫系统攻击胰岛β细胞,导致胰岛素生产障碍。现有的治疗方法如胰岛素注射不能根治疾病,而目前的疫苗研发仍处于初级阶段。因此,开发新的治疗策略,特别是能够调节免疫系统并恢复免疫耐受的方法,对于改善T1D患者的治疗效果具有重要意义。此项研究展示了tFNAs在调节免疫反应中的潜力,为糖尿病的预防和治疗提供了新的方向。
前沿科研成果:本研究展示了tFNAs在预防T1D中的潜力,其通过增加调节性T细胞(Tregs)并抑制自身反应性T细胞,有效维护胰岛β细胞功能和正常血糖水平。
本研究发现tFNAs能在NOD小鼠中诱导免疫耐受,维持正常血糖水平,减少糖尿病的发病率。tFNAs治疗能够提高调节性T细胞(Tregs)的频率,并抑制自身反应性T细胞,从而保护β细胞,防止T1D的发生。
实验方法:
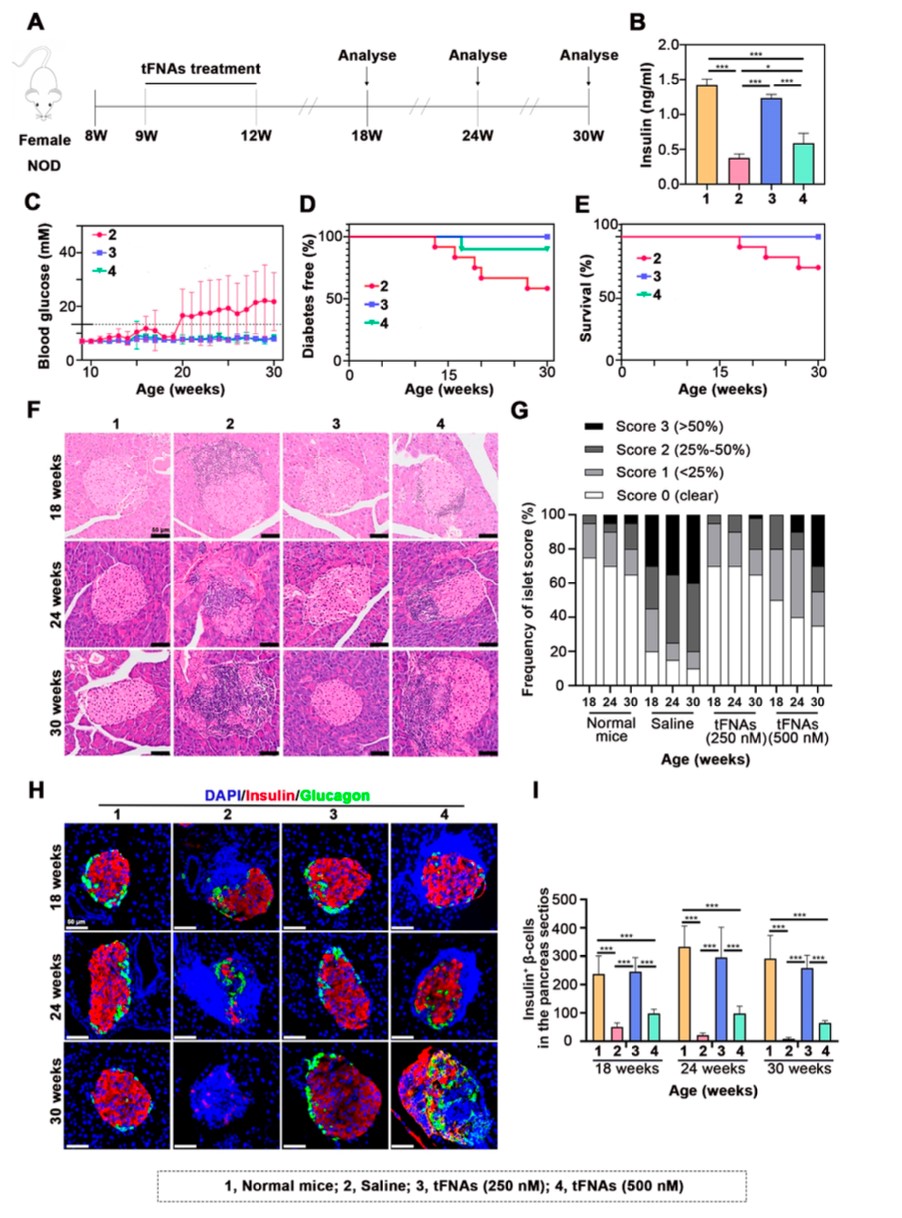
在本研究中,我们采用了非肥胖糖尿病(NOD)小鼠作为1型糖尿病(T1D)的动物模型,并通过尾静脉注射的方式给予小鼠不同浓度的四面体框架核酸(tFNAs),以评估其对T1D发病的预防效果。实验设计包括监测小鼠在治疗前后的血糖水平,使用免疫组化和流式细胞术来分析小鼠胰岛和免疫系统中的细胞变化,特别是调节性T细胞(Tregs)和自身反应性T细胞的数量及活性。此外,通过定期收集和分析小鼠的血清样本,检测胰岛β细胞功能相关的生物标志物,以全面评估tFNAs的免疫调节作用及其在预防T1D中的潜在效果。这些方法的综合运用旨在深入理解tFNAs如何通过免疫调节机制来阻止糖尿病的发展。
实验结果:
在本研究中, tFNAs的应用在NOD小鼠模型中显示出显著的治疗效果。实验结果表明,tFNAs处理的小鼠在整个研究期间维持了正常的血糖水平,并且与对照组相比,糖尿病的发病率显著降低。免疫组化和流式细胞术的数据揭示了tFNAs能够显著增加调节性T细胞(Tregs)的比例,同时抑制自身反应性T细胞的活性,这一变化有助于保护胰岛β细胞免受免疫攻击。此外,通过对胰岛组织的定期检查,我们发现tFNAs处理组中β细胞的质量和功能得到了保留和改善。这些结果不仅证明了tFNAs在预防T1D中的有效性,还突显了其作为免疫调节剂在治疗自身免疫性疾病中的潜力。
研究结论:
FNAs通过调节免疫反应,诱导免疫耐受,为预防自身免疫性1型糖尿病提供了一种新的治疗策略。这些发现强调了tFNAs在自身免疫性疾病预防和治疗中的潜在应用。
发表文献:Nano Letters 2021, 21, 4437−4446. DOI: 10.1021/acs.nanolett.1c01131
![]() Tetrahedral Framework Nucleic Acids Induce Immune Tolerance and Prevent the Onset of Type 1 Diabetes
Tetrahedral Framework Nucleic Acids Induce Immune Tolerance and Prevent the Onset of Type 1 Diabetes